企业动态
塔吉瑞慢粒第四代 Bcr-Abl 抑制剂临床申请获 CDE 受理
2020-04-13 浏览量:
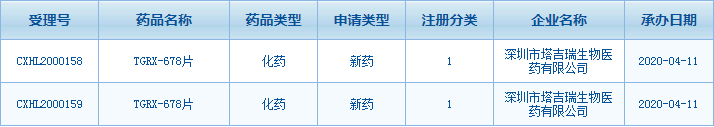
由深圳市塔吉瑞生物医药有限公司自主研发的第四代 Bcr-Abl 抑制剂 TGRX-678 临床试验申请,于 2020 年 4 月 11 日经 CDE(国家药监局药审中心)正式受理。该药主要用于慢性粒细胞白血病的治疗。临床前研究显示,TGRX-678 对于临床现有的耐药,特别是 T315I 守门残基突变,具有很高的活性。
不同于前三代 Bcr-Abl 抑制剂,TGRX-678 采用全新的作用机制,具有极佳的选择性,可以很好的作用于现有的耐药突变。同时,临床前的动物实验显示其毒副作用极低,预测治疗窗口十分可观。

2018 年电影《我不是药神》的热映,将慢性粒细胞白血病和癌症患者用药难的现状带入大众的视野。电影中没有提到的是,“神药”在服用一段时间之后会因病人产生耐药而失效,病人需要不断更换新一代的药物,才能长期生存。目前国际上唯一获批的第三代药 Ponatinib 是塔吉瑞创始人、董事长王义汉博士在美国制药公司 ARIAD 工作时,和同事们一起历十余年努力开发出来的。然而遗憾的是,虽然 Ponatinib 早在 2012 年就被 FDA 获批上市,却至今没有进入到国内。电影热播后,多家媒体争相对王义汉博士进行了采访,字里行间可见王博士为挽救癌症患者生命的使命感,和带领塔吉瑞研发全球领先的中国本土创新药的决心。
详情请看《王义汉:我不是药神,我是科研路上的追梦人》、《王义汉:“我不是药神,我只想给他们生的希望”》、《塔吉瑞王义汉:格列卫之后,打造新一代抗癌银弹》
塔吉瑞是一家专注于研发最新一代小分子靶向抗癌药的生物医药公司,致力于挑战癌症获得性耐药的重大医学难题。塔吉瑞通过核心技术手段,设计合成高度专一的抗耐药活性分子。成立至今,公司已经申报专利多达 100 余项。除 TGRX-678 外,公司主要在研产品还有针对 ALK 阳性非小细胞肺癌的第三代产品,也将于近期递交临床试验申请。
“伯”揽人才,闻天下“仕”。在此也诚挚地欢迎更多拥有共同愿景的伙伴们加入我们的团队,一起努力攻关,力争把革命性的创新疗法尽早带给病人。(详情请看:《2020年,塔吉瑞生物等你来加入!》)







 联系电话:+86-0755-86934300
联系电话:+86-0755-86934300 地址:深圳市南山区科兴科学园 A1 单元 3 楼
地址:深圳市南山区科兴科学园 A1 单元 3 楼 邮箱:
邮箱: